- Автор Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:33.
- Последно модифициран 2025-01-22 16:56.
Топлина на образуване . Топлина на образуване , наричан още стандартен топлина на образуване , образуване на енталпия , или стандартно енталпия на образуване , размерът на топлина абсорбира или еволюира, когато един мол от съединение се образува от съставните му елементи, като всяко вещество е в нормалното си физическо състояние (газ, течност или твърдо вещество).
Освен това, какво означава топлината на образуване?
в химията, топлина на образуване е топлина освободен или абсорбиран ( енталпия промяна) по време на образуване на чисто вещество от неговите елементи при постоянно налягане (в техните стандартни състояния). Образуване на топлина обикновено се обозначава с ΔHе. Обикновено се изразява в единици килоджаули на мол (kJ/mol).
Също така, какво е топлината на образуване на водата? Водород и кислород се комбинират, за да се образуват вода . Подобно на други реакции, те са придружени или от усвояване, или от освобождаване на топлина . Стандарт топлина на образуване isthe енталпия промяна, свързана с образуване от един мол съединение от неговите елементи в техните стандартни състояния.
Човек може също да попита каква е топлината на образуване на елемент в неговото стандартно състояние?
В стандартна енталпия на образуване за елемент в неговото стандартно състояние е НУЛА!!!! Елементи в техните стандартно състояние не се формират, те просто са. И така, ΔH°е за C (s, графит) е нула, но ΔH°е за C (s, диамант) е 2 kJ/mol. Това е, защото графитът е стандартно състояние за въглерод, а не за диамант.
Какво е определението за топлина на реакция?
Определение за топлина на реакцията .: на топлина еволюира или абсорбира по време на химикал реакция поемане при условия на постоянна температура и на постоянен обем или по-често постоянно налягане, особено: количеството, което участва, когато грам еквиваленти на веществата влизат в реакция.
Препоръчано:
Какъв е процесът на образуване на решение?

Разтвор се получава, когато едно вещество, наречено разтворено вещество, се „разтваря“в друго вещество, наречено разтворител. Разтварянето е, когато разтвореното вещество се разпада от по-голям кристал от молекули на много по-малки групи или отделни молекули. Те правят това, като отдръпват йоните и след това заобикалят молекулите на солта
Какви са етапите на образуване на звезда?
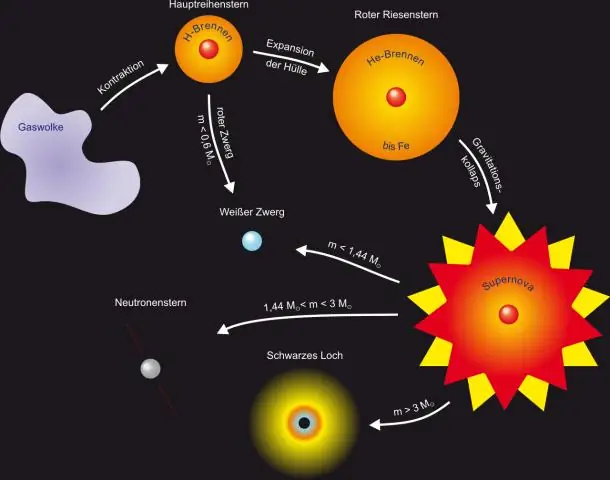
7 основни етапа на звезда Гигантски газов облак. Звездата започва живота като голям облак от газ. Протозвезда е бебе звезда. Фаза Т-Таури. Звезди от основната последователност. Разширяване в Червен гигант. Сливане на по-тежки елементи. Свръхнови и планетарни мъглявини
Каква е стандартната енталпия на образуване на серен диоксид?

За проверка трябва да бъде (−296,81±0,20) kJ/mol. Трябва да използвате NIST по-често. Всъщност получих −310,17 kJ/mol. Първо трябва да потърсите ΔH∘f за SO3(g)
Каква е енталпията на образуване на Cao?

Таблица на топлината на образуване на съединение ΔHf (kJ/mol) CaCO3 -1207,0 CaO(s) -635,5 Ca(OH)2(s) -986,6 CaSO4(s) -1432,7
Защо енталпията на образуване на елементите е нула?

Енталпията на образуване за елемент в неговото елементарно състояние винаги ще бъде 0, тъй като не е необходима енергия за образуване на естествено срещащо се съединение. Когато веществото се образува от най-стабилната форма на неговите елементи, настъпва промяна в енталпията
