
- Автор Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:33.
- Последно модифициран 2025-01-22 16:56.
Редуциращи агенти може да бъде класиран чрез увеличаване на силата чрез класиране техен намаляване потенциали. В редуциращ агент е по-силен, когато има по-отрицателен намаляване потенциал и по-слаб, когато има по-положителен намаляване потенциал.
По подобен начин може да попитате как идентифицирате окислителите и редуциращите агенти?
А редуциращ агент е вещество, което причинява на друго вещество намаляват . Така че да идентифицират ан окислител , просто погледнете окислителното число на атома преди и след реакцията. Ако степента на окисление е по-голяма в продукта, тогава той губи електрони и веществото се окислява.
Освен това, кои елементи са добри редуциращи агенти? Добрите редуциращи агенти включват активните метали, като напр натрий , магнезий , алуминий и цинк, които имат относително малка йонизационна енергия и ниски електроотрицателни стойности. Метални хидриди, като NaH, CaH2и LiAlH4, които официално съдържат H- йон, също са добри редуциращи агенти.
Също така въпросът е как намирате най-слабия редуктор?
Обяснение: Ето една типична таблица със стандарти намаляване потенциали. Видовете в горния ляв ъгъл имат най-голям „потенциал“да бъдат намалени, така че те са най-силно окисляващи агенти . Най-силното окисляване агент в списъка е F2, следван от H2O2 и така нататък до най-слабите окисляващи агент , Li+.
Силен редуктор ли е HCl?
HCl (Cl^-) може да се окисли до хлорен газ (реакция на Дийкон) с помощта на a по-силен окисляващи агент отколкото HCl (TiO2). HCl (H^+) може да се редуцира до газообразен водород чрез по-слабо окисляване агент отколкото HCl ( по-силен редуктор ) като Zn. Няма крайно окисляване агент или редуциращ агент.
Препоръчано:
Как оценявате съставните функции?
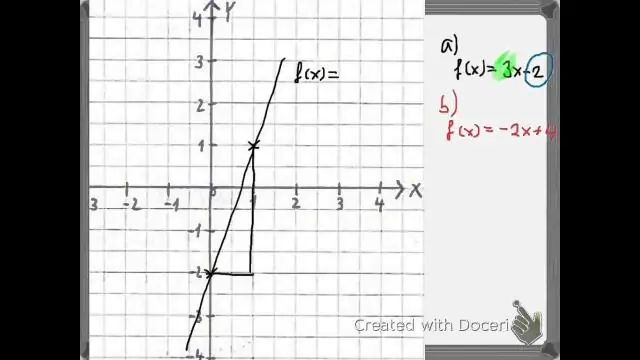
Оценяване на съставни функции с помощта на графики Намерете дадения вход към вътрешната функция по оста x на нейната графика. Отчетете изхода на вътрешната функция от оста y на нейната графика. Намерете изхода на вътрешната функция по оста x на графиката на външната функция
Кой е най-често използваният дехидратиращ агент?

Химикалите, които обикновено се използват като дехидратиращи агенти, включват концентрирана фосфорна киселина, концентрирана сярна киселина, гореща керамика и горещ алуминиев оксид
Какво е дехидратиращ агент с пример?

Химикалите, които обикновено се използват като дехидратиращи агенти, включват концентрирана фосфорна киселина, концентрирана сярна киселина, гореща керамика и горещ алуминиев оксид. Реакцията на дехидратация е същата като синтеза на дехидратация
Как оценявате размера на популацията в метода за повторно улавяне?

Техниката Mark-Recapture се използва за оценка на размера на популацията, когато е непрактично да се преброят всеки индивид. Основната идея е, че улавяте малък брой индивиди, поставяте безобиден знак върху тях и ги пускате обратно в популацията
Как оценявате пи?

Обиколката на окръжност се намира с формулата C= π*d = 2*π*r. Така пи е равно на обиколката на окръжността, разделена на неговия диаметър. Включете числата си в калкулатор: резултатът трябва да бъде приблизително 3,14. Повторете този процес с няколко различни кръга и след това осреднете резултатите
