
- Автор Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:33.
- Последно модифициран 2025-01-22 16:56.
Ензимите са протеини, които са способен да намали енергията на активиране за различни биохимични реакции . Ензим катализаAn ензимът катализира биохимична реакция чрез свързване на субстрат в активното място. След реакция е продължил, продуктите са освободен и на ензимът може да катализира по-нататък реакции.
По подобен начин се пита каква е ролята на ензима в биохимичната реакция?
В организмите катализаторите се наричат ензими . по същество, ензими са биологични или органични катализатори. Ан ензим е протеин, който ускорява а биохимична реакция . Ан ензим работи чрез намаляване на количеството енергия на активиране, необходимо за стартиране на реакция.
Освен това, какво е биохимичен катализатор? А катализатор е нещо, което позволява на реакцията да се случи по-лесно, отколкото би се случило при нейно отсъствие. Биохимични катализатори често са големи протеинови молекули, наречени ензими, които свързват субстрат в изкривена ориентация, която „излага“връзката на прекъсване.
Следователно, каква е химическата основа на ензимната катализа?
Ензимна катализа е увеличаването на скоростта на процеса от биологична молекула, ензим „Повечето ензими са протеини и повечето такива процеси са химически реакции. В рамките на ензим , в общи линии катализа се случва на локализирано място, наречено активно място.
Какво се случва с ензим след биохимична реакция?
В ензим ускорява реакция чрез намаляване на енергията на активиране, необходима за реакция да започна. Сравнете енергията на активиране със и без ензим . Ензими като цяло по-ниска енергия на активиране чрез намаляване на енергията, необходима за обединяването на реагентите и реагират.
Препоръчано:
При каква температура ензимът каталаза функционира най-добре?

Да, каталазата работи най-добре при неутрално pH и температура от 40 °C, като и двете са близки до състоянието на тъканите на бозайници
Какво означава ензимът да е ефективен?

Увеличаването на скоростта на реакцията на химическа реакция позволява реакцията да стане по-ефективна и следователно повече продукти се генерират с по-бърза скорост. Това е известно като каталитична ефективност на ензимите, която чрез увеличаване на скоростта води до по-ефективна химическа реакция в рамките на биологичната система
Какво разбирате под преходна реакция и стабилна реакция?

Преходна реакция След прилагане на вход към системата за управление, изходът отнема известно време, за да достигне стабилно състояние. Така изходът ще бъде в преходно състояние, докато не премине в стационарно състояние. Следователно реакцията на системата за управление по време на преходно състояние е известна като преходна реакция
Какво е името на ензима, който катализира синтеза на веригата на иРНК?
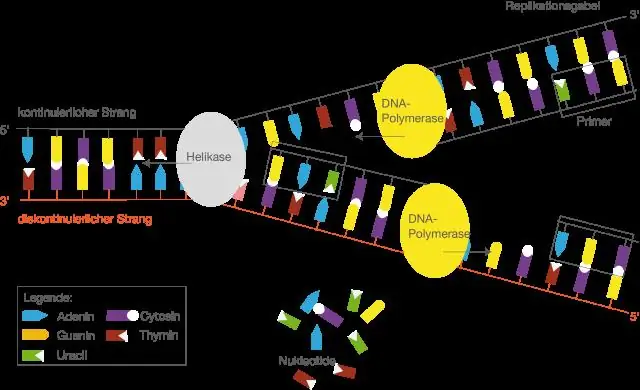
ТРНК е "пратена" РНК. иРНК се синтезира в ядрото, като се използва нуклеотидната последователност на ДНК като матрица. Този процес изисква нуклеотидни трифосфати като субстрати и се катализира от ензима РНК полимераза II. Процесът на производство на иРНК от ДНК се нарича транскрипция и се случва в ядрото
Какво се случва, ако ензимът не работи?

Ако средата около ензима стане твърде киселинна или твърде основна, формата и функцията на ензима ще страдат. Химикалите, наречени инхибитори, също могат да попречат на способността на ензима да предизвика химическа реакция. Инхибиторите могат да се появят естествено. Те също могат да се произвеждат и произвеждат като лекарства
